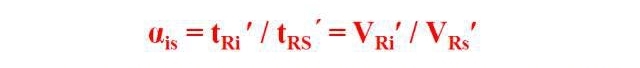Chromatographie, och bekannt als "chromatographesch Analyse", "Chromatographie", ass eng Trennungs- an Analysemethod, déi eng ganz breet Palette vun Uwendungen an der analytescher Chimie, der organescher Chimie, der Biochemie an anere Beräicher huet.
De Grënner vun der Chromatographie ass e russesche Botaniker M.Tsvetter.1906 huet de russesche Botaniker Zvetter d'Resultater vu sengem Experiment publizéiert: Fir Pflanzenpigmenter ze trennen, huet hien Petroleumetherextrakt mat Planzenpigmenter an e Glasröhr mat Kalziumkarbonatpulver gegoss an et mat Petroleumether vun uewe bis ënnen eluéiert.Well verschidde Pigmenter verschidden Adsorptiounskapazitéiten op der Uewerfläch vu Kalziumkarbonatpartikelen hunn, mam Prozess vun der Ausleechung, beweegen sech verschidde Pigmenter mat verschiddene Geschwindegkeeten erof, sou datt Bande vu verschiddene Faarwen bilden.D'Pigmentkomponente goufen getrennt.Hien huet dës Trennungsmethod Chromatographie genannt.
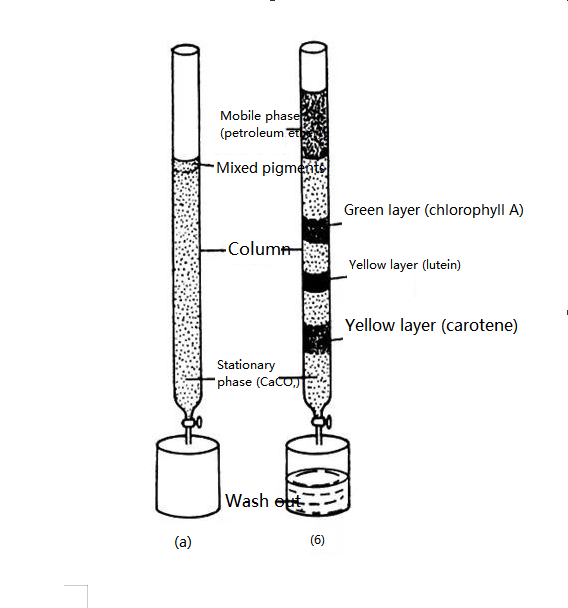
Schematesch Representatioun vun engem Planz Blat Pigment Trennung Experiment
Mat der kontinuéierlecher Entwécklung vun Trennungsmethoden ginn ëmmer méi faarweg Substanzen den Objet vun der Trennung, d'Chromatographie huet och no an no d'Bedeitung vu "Faarf" verluer, awer den Numm gëtt haut nach benotzt.
Chromatographesch Klassifikatioun
D'Essenz vun der Chromatographie ass e Prozess an deem d'Moleküle, déi ze trennen, opgedeelt a equilibréiert sinn tëscht der stationärer Phase an der mobiler Phase.Verschidde Substanze ginn ënnerschiddlech tëscht den zwou Phasen opgedeelt, wat se mat verschiddene Geschwindegkeete mat der mobiler Phase mécht.Mat der Bewegung vun der mobiler Phase gi verschidde Komponenten an der Mëschung vuneneen op der stationärer Phase getrennt.Ofhängeg vum Mechanismus, kann et a verschidde Kategorien opgedeelt ginn.
1, no der zwee-Phase kierperlech Staat Klassifikatioun
Mobil Phase: Gaschromatographie, Flëssegchromatographie, Superkritesch Flëssegchromatographie
Stationär Phase: Gas-fest, Gas-Flësseg;Flësseg-fest, flësseg-flësseg
2, no der Form vun stationärer Phase Klassifikatioun
Kolonnchromatographie: gepackte Kolonnchromatographie, Kapillarkolonnechromatographie, Mikropacked Kolonnechromatographie, präparativ Chromatographie
Fligerchromatographie: Pabeierchromatographie, Dënnschichtchromatographie, Polymermembranchromatographie
3, klasséiert no der Trennung Mechanismus
Adsorptionchromatographie: Verschidde Komponente ginn getrennt no hirer Adsorptiouns- an Desorptiounskapazitéit op Adsorbenten
Partition Chromatography: Déi verschidde Komponente gi getrennt no hirer Solubilitéit am Léisungsmëttel
Molekulare Ausgrenzungschromatographie: no der Gréisst vun der molekulare Gréisst vun der Trennung ln Ionenaustauschchromatographie: verschidde Bestanddeeler vun der Affinitéit fir d'Ionenaustauschharz-Trennung
Affinitéitschromatographie: Trennung mat der Präsenz vun enger spezifescher Affinitéit tëscht biologesche Makromolekülen
Kapillär Elektrophorese: d'Komponente goufen getrennt no den Ënnerscheeder an der Mobilitéit an / oder Partitionverhalen
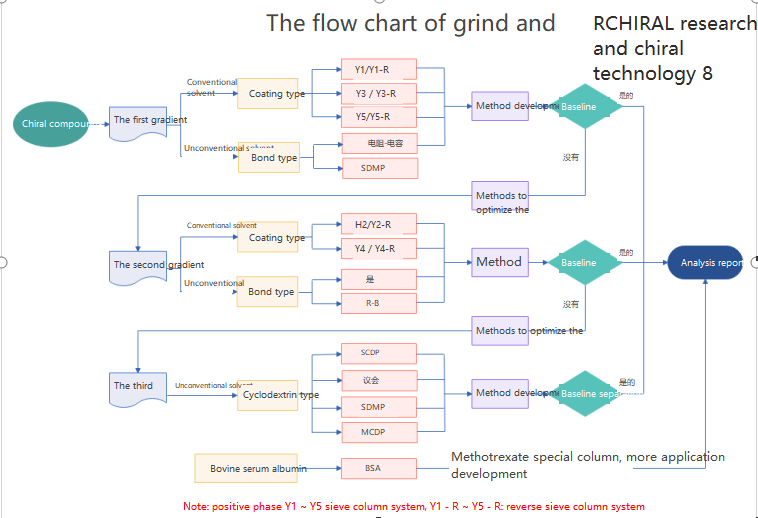
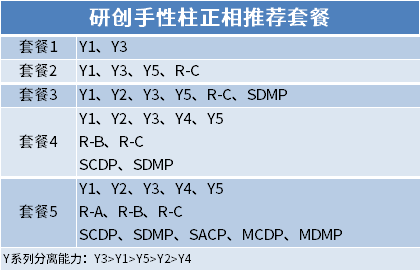
Chiral Chromatographie gëtt fir d'Trennung an d'Analyse vu chiralen Drogen benotzt, déi an dräi Kategorien opgedeelt kënne ginn: chiral Derivatiounsreagensmethod;Chiral mobil Phase Additiv Method;Chiral stationär Phase Resolutioun Method
Basis Terminologie fir Chromatographie
D'Kéiren, déi kritt ginn andeems d'Äntwertsignale vun de Komponenten no der Detektioun vun der chromatografescher Trennung géint d'Zäit geplot ginn, ginn Chromatogramme genannt.
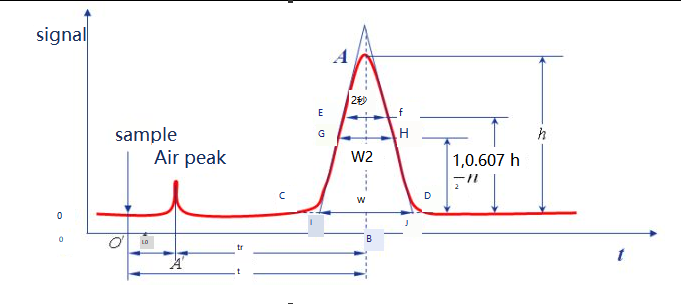
Baseline:Ënner bestëmmte chromatographesche Bedéngungen gëtt d'Kurve vum Signal generéiert wann nëmmen déi mobil Phas duerch den Detektorsystem passéiert, d'Basislinn genannt, wéi an der ot-Linn gewisen.Wann den experimentellen Zoustand stabil war, war d'Basislinn eng Linn parallel zu der horizontaler Achs.D'Basislinn reflektéiert de Kaméidi vum Instrument, haaptsächlech dem Detektor, mat der Zäit.
Héicht Héicht:déi vertikal Distanz tëscht dem chromatografeschen Héichpunkt an der Baseline, mat h bezeechent, wéi an der AB 'Linn gewisen.
Regioun Breet:D'Regiounsbreet vum chromatographesche Peak ass direkt mat der Trennungseffizienz verbonnen.Et ginn dräi Methoden fir chromatographesch Peak Breet ze beschreiwen: Standarddeviatioun σ, Peak Breet W, an FWHM W1/2.
Standarddeviatioun (σ):σ ass déi hallef Distanz tëscht den zwee Inflektiounspunkten op der normaler Verdeelungskurve, an de Wäert vun σ weist de Grad vun der Dispersioun vun de Komponenten ewech vun der Kolonn un.Wat de Wäert vun σ méi grouss ass, dest méi dispergéiert d'Effluentkomponenten, an dest méi schlëmm ass den Trennungseffekt.Ëmgekéiert sinn d'Effluentkomponenten konzentréiert an d'Trennungseffekt ass gutt.
Peak Breet W:D'Kräizungspunkte op béide Säiten vum chromatographesche Peak ginn als Tangentlinne benotzt, an den Ofschnëtt op der Basislinn gëtt Peakbreed oder Baseline Breet genannt, wat och als W ausgedréckt ka ginn, wéi an der Figur IJ gewisen.Laut dem Prinzip vun der normaler Verdeelung kann d'Relatioun tëscht Spëtzbreed an Standardabweichung als W = 4σ bewisen ginn.
W1/2:D'Spëtzt Breet an der Halschent vun der Héicht gëtt FWHM genannt, wéi fir d'Distanz vum GH gewisen.W1/2=2.355σ, W=1.699W1/2.
W1/2, W gi béid ofgeleet vu σ a gi benotzt fir Peakberäicher ze berechnen zousätzlech fir de Kolonneffekt ze moossen.FWHM Messung ass méi bequem an am meeschte benotzt.
kuerze Resumé
Vun der chromatographescher Peak Ausflusskurve kënnen déi folgend Ziler erreecht ginn:
eng, qualitativ Analyse war baséiert op der Retention Wäert vun chromatographic Biergspëtzten gesuergt
b, quantitativ Analyse baséiert op der Fläch oder Peak vum chromatographesche Peak
C. D'Trennungseffizienz vun der Kolonn gouf no dem Retentiounswäert an der Spëtzt Breet vun der chromatographescher Héichpunkt bewäert.
D'Berechnungsformel involvéiert an der Chromatographie
1. Retention Wäert
De Retentiounswäert ass e Parameter dee benotzt gëtt fir de Grad ze beschreiwen an deem e Probekomponent an der Kolonn behalen gëtt an als Indikator fir chromatographesch Charakteriséierung benotzt gëtt.Seng Representatiounsmethod ass wéi follegt:
Retentiounszäit tR
Zäit vum DoudtM
Ajustéiert d'Retentiounszäit tR'=tR-tM
(Gesamtzäit an der stationärer Phase)
Volume vun Retention
VR=tR*F.(onofhängeg vun der mobiler Phasevitesse)
Doudeger Volumen
VM=tM*Fc
(De Raum net besat vun der stationärer Phase am Flowwee vum Injektor zum Detektor)
Ajustéiert de Retentiounsvolumen VR'=t'R*Fc
2. Relativ Retention Wäert
Relative Retentiounswäert, och bekannt als Trennungsfaktor, Partitionskoeffizientverhältnis oder Relativ Kapazitéitsfaktor, ass de Verhältnis vun der ugepasster Retentiounszäit (Volumen) vun der getester Komponent an der ugepasst Retentiounszäit (Volumen) vum Standard ënner bestëmmte chromatographesche Bedéngungen.

Relativ Retentiounswäerter goufen benotzt fir den Afloss vu bestëmmte Betribsbedéngungen ze eliminéieren, sou wéi Flowrate a Fixativverloscht, op Retentiounswäerter.De Standard am relativen Retentiounswäert kann e Bestanddeel an der getester Probe sinn oder eng Verbindung kënschtlech bäigefüügt.
3. Retentioun Index
De Retentiounsindex ass den Retentiounsindex vun der Substanz i, déi an enger fixer Léisung X getest gëtt. Als Referenzstoffer ginn zwee n-Alanen ausgewielt, vun deenen eng N Kuelestoffzuel huet an déi aner N+n.Hir ugepasst Retentiounszäit ass t 'r (N) respektiv t 'r (N+n), sou datt déi ugepasst Retentiounszäit t 'r (i) vun der Substanz i, déi getest gëtt, genee tëscht hinnen ass, dat heescht, t'r (N).
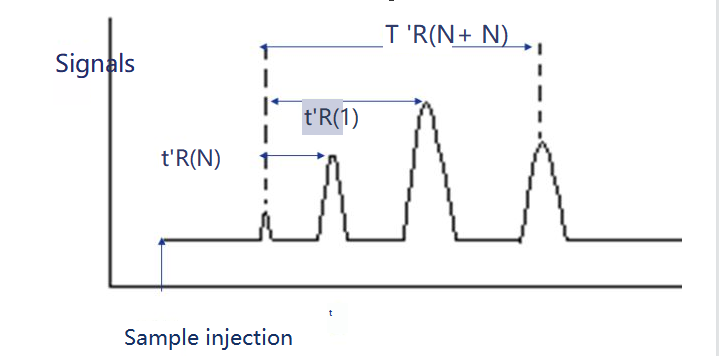
De Retentiounsindex ka wéi follegt berechent ginn.
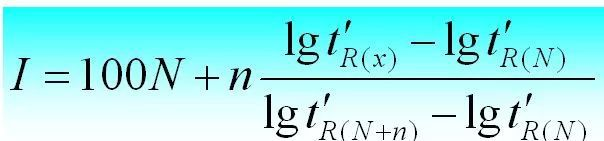
4. Kapazitéit Faktor (k)
Am Gläichgewiicht ass de Verhältnis vun der Mass vun engem Komponent an der stationärer Phase (s) an der mobiler Phase (m), de Kapazitéitsfaktor genannt.D'Formel ass wéi follegt:
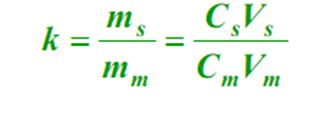
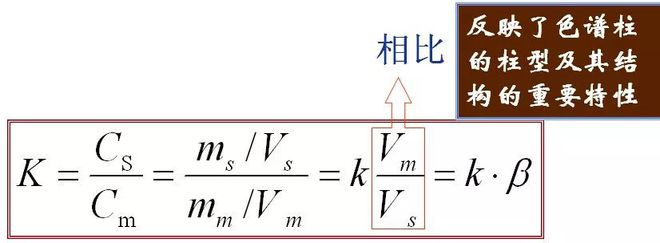
5、Partitionskoeffizient (K) Am Gläichgewiicht ass de Verhältnis vun der Konzentratioun vun engem Komponent an der stationärer Phase (s) an der mobiler Phase (m), genannt Partitionskoeffizient.D'Formel ass wéi follegt

D'Relatioun tëscht K an K:
Et reflektéiert de Kolonn Typ a seng Knot wichteg Eegeschafte vun Struktur
kuerze Resumé
Relatioun tëscht Retentiounswäert a Kapazitéitsfaktor a Partitionskoeffizient:
Chromatographesch Trennung baséiert op den Ënnerscheed an der Adsorptioun oder Opléisungsfäegkeet vun all Komponent an enger fixer relativer Probe, déi quantitativ duerch d'Gréisst vum Partitionskoeffizient K (oder Kapazitéitsfaktor k) Wäert ausgedréckt ka ginn.
D'Komponente mat staarker Adsorptioun oder Opléisungsfäegkeet hunn e grousse Partitionskoeffizient (oder Kapazitéitsfaktor) a laang Retentiounszäit.Ëmgekéiert hunn d'Komponente mat schwaacher Adsorptioun oder Solubilitéit e klenge Partitionskoeffizient an eng kuerz Retentiounszäit.
Basis Theorie vun der Chromatographie
1. Schacht Theorie
(1) Virausgesat - thermodynamesch Theorie
Et huet ugefaang mam Tuermplackmodell, dee vum Martin a Synge proposéiert gouf.
Fractionating Kolonn: am Schacht fir e puer Mol vun Gas-Flëssegkeet Gläichgewiicht, no dem Kachpunkt vun der verschidden Trennung.
Kolonn: D'Komponente gi vu multiple Partitionen tëscht den zwou Phasen ausgeglach a getrennt no verschiddene Partitionskoeffizienten.
(2) Hypothese
(1) Et gi vill Schachtelen an der Kolonn, an d'Komponente kënne séier d'Verdeelungsgläichgewiicht am Schachtintervall erreechen (dat ass d'Héicht vum Schacht).
(2) Déi mobil Phase geet an d'Kolonn, net kontinuéierlech awer pulséierend, dat heescht, all Passage ass e Kolonnvolumen.
(3) Wann d'Probe op all Kolonnplack bäigefüügt gouf, konnt d'Diffusioun vun der Probe laanscht d'Kolonnachs vernoléissegt ginn.
(4) De Partitionskoeffizient ass gläich op all Schacht, onofhängeg vun der Quantitéit vun de Komponenten.Dat ass, de Partitionskoeffizient ass konstant op all Taban.
(3) Prinzip
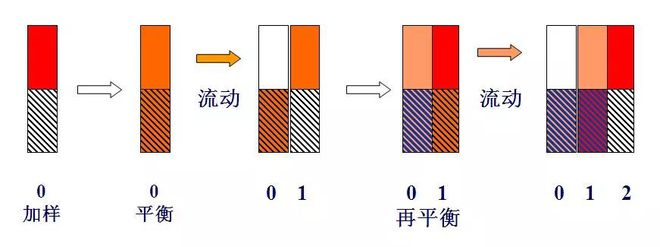
Schematesch Diagramm vun der Schachttheorie
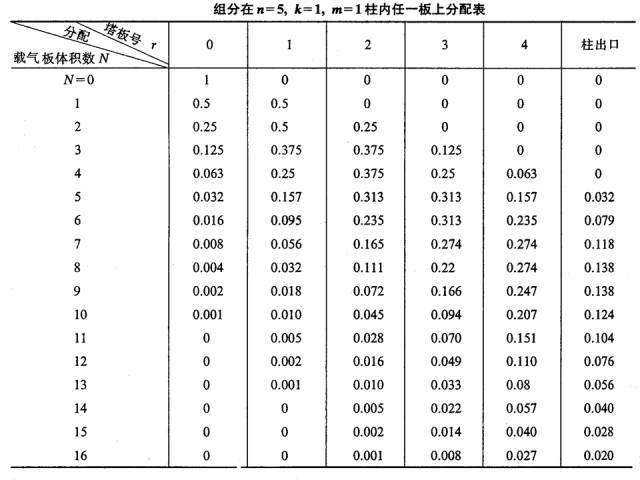
Wann e Bestanddeel vun Eenheet Mass, nämlech m = 1 (zum Beispill, 1mg oder 1μg), gëtt op d'Nummer 0 Schacht dobäi, an no Verdeelung Gläichgewiicht, well k = 1, nämlech ns = nm, nm = ns = 0,5.
Wann e Plackevolumen (lΔV) vum Trägergas an der Plack 0 a Form vun der Pulsatioun erakënnt, gëtt den Trägergas, deen den nm Komponent an der Gasphase enthält, op d'Plack 1 gedréckt. an der nm Komponent an der Gas Phase vun Plack 1 gëtt tëscht den zwou Phasen ëmverdeelt ginn.Dofir ass de Gesamtbetrag vun de Komponenten, déi an der Plack 0 enthale sinn, 0,5, an där d'Gas- a Flëssegphasen all 0,25 sinn, an de Gesamtbetrag an der Plack 1 ass och 0,5.D'Gas- a Flëssegkeetsphase waren och 0,25.
Dëse Prozess gëtt widderholl all Kéier wann en neie Plackvolumen-Trägergas an d'Kolonn pulséiert gëtt (kuckt d'Tabell hei ënnen).
(4) Chromatographesch Ausfluss Curve Equatioun

σ ass d'Standarddeviatioun, ass d'Retentiounszäit, C ass d'Konzentratioun zu all Moment,
C, ass d'Injektiounskonzentratioun, dat heescht de Gesamtbetrag vun de Komponenten (Peakberäich A).
(5) Kolonne Effizienz Parameteren
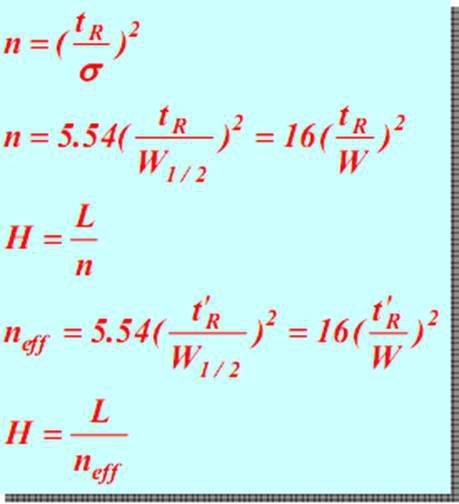
Bei enger konstanter tR, déi méi kleng W oder w 1/2 (dat ass, de méi schmuel Peak), déi méi grouss d'Zuel vun theoretesch Placke n, déi méi kleng der theoretesch Plack Héicht, a méi héich d'Trennungseffizienz vun der Kolonn.Datselwecht ass wouer fir den effektiven Theorie Schacht neff.Dofir ass déi theoretesch Zuel vun de Schacht en Index fir d'Effizienz vun de Sailen ze evaluéieren.
(5) Charakteristiken a Mängel
> Virdeeler
D'Schachttheorie ass semi-empiresch an erkläert d'Form vun der Ausflusskurve
D'Partitionéierungs- an Trennungsprozesser vun de Komponente ginn illustréiert
En Index fir d'Effizienz vun der Kolonn ze evaluéieren gëtt proposéiert
> Aschränkungen
D'Komponente kënnen net wierklech d'Verdeelungsgläichgewiicht an den zwou Phasen erreechen:
Längsdiffusion vun Komponenten an der Kolonn kann net ignoréiert ginn:
Den Afloss vu verschiddene kinetesche Faktoren op de Massentransferprozess gouf net berücksichtegt.
D'Relatioun tëscht Kolonneffekt a Stroumgeschwindegkeet vun der mobiler Phase kann net erkläert ginn:
Et ass net kloer wéi eng Haaptfaktoren de Kolonneffekt beaflossen
Dës Problemer sinn zefriddestellend an der Taux Theorie geléist.
2. Taux Theorie
1956 hunn den hollännesche Geléiert VanDeemter et al.d'Konzept vun der Schachttheorie absorbéiert, a kombinéiert déi kinetesch Faktoren, déi d'Héicht vum Schacht beaflossen, d'kinetesch Theorie vum chromatographesche Prozess-Rate-Theorie virgestallt an d'VanDeemter Equatioun ofgeleet.Et betruecht de chromatographesche Prozess als en dynamesche Net-Gläichgewiichtprozess a studéiert den Afloss vu kinetesche Faktoren op d'Spëtzeverbreedung (dh Kolonneffekt).
Spéider, Giddings and Snyder et al.proposéiert d'Flëssegchromatographie Taux Equatioun (nämlech Giddings Equatioun) baséiert op der VanDeemter Equatioun (spéider Gas Chromatography Taux Equatioun genannt) an no der Eegeschafte Ënnerscheed tëscht Flëssegket a Gas.
(1) Van Deemter Equation
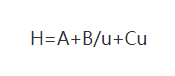
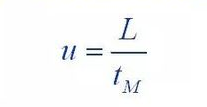
Wou: H: ass d'Héicht vum Board
A: Koeffizient vun Eddy Diffusioun Begrëff
B: Koeffizient vun der molekulare Diffusioun Begrëff
C: Koeffizient vun der Mass Transfermaart Resistenz Begrëff
(2) Giddings Equatioun
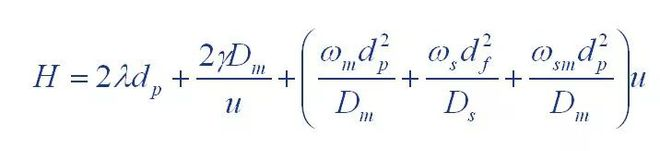
Quantitativ a qualitativ Analyse
(1) Qualitativ Analyse
Qualitativ chromatografesch Analyse ass d'Verbindungen ze bestëmmen déi vun all chromatographesche Peak vertruede sinn.Well verschidde Substanzen definitive Retentiounswäerter ënner bestëmmte chromatographesche Bedéngungen hunn, kann de Retentiounswäert als qualitativen Index benotzt ginn.Verschidde chromatographesch qualitativ Methoden baséieren momentan op Retentiounswäerter.
Wéi och ëmmer, verschidde Substanzen kënnen ähnlech oder identesch Retentiounswäerter ënner de selwechte chromatographesche Bedéngungen hunn, dat heescht, d'Retentiounswäerter sinn net exklusiv.Also ass et schwéier eng komplett onbekannte Probe ze charakteriséieren op Basis vu Retentiounswäerter eleng.Wann op der Basis vum Verständnis vun der Quell, der Natur an dem Zweck vun der Probe, kann e virleefeg Uerteel vun der Zesummesetzung vun der Probe gemaach ginn, an déi folgend Methoden kënne benotzt ginn fir d'Verbindung ze bestëmmen, déi vum chromatographesche Peak vertruede sinn.
1. Qualitativ Kontroll mat reinen Substanzen
Ënner bestëmmte chromatographesche Bedéngungen huet en Onbekannt nëmmen eng definéiert Retentiounszäit.Dofir kann dat Onbekannt qualitativ identifizéiert ginn andeems d'Retentiounszäit vun der bekannter reiner Substanz ënner de selwechte chromatographesche Bedéngungen mat der Retentiounszäit vun der onbekannter Substanz vergläicht.Wann déi zwee d'selwecht sinn, kann déi onbekannt Substanz eng bekannte reng Substanz sinn;Soss ass dat Onbekannt net déi reng Substanz.
Déi reng Substanz Kontrollmethod ass nëmme fir déi onbekannt Substanz applicabel, deem seng Zesummesetzung bekannt ass, deem seng Zesummesetzung relativ einfach ass, an deem seng reng Substanz bekannt ass.
2. Relativ Retention Wäert Method
De relativen Retentiounswäert α bezitt sech op d'Upassung tëscht Komponent i a Referenzmaterial Verhältnis vu Retentiounswäerter:
Et ännert sech nëmme mat der Ännerung vun der Fixativ a Kolonntemperatur, an huet näischt mat anere Betribsbedéngungen ze dinn.
Bei enger bestëmmter stationärer Phase a Kolonntemperatur ginn déi ugepasst Retentiounswäerter vum Komponent i a Referenzstoff s respektiv gemooss, an dann no der uewe genannter Formel berechent.Déi erhalen relativ Retentiounswäerter kënne qualitativ mat den entspriechende Wäerter an der Literatur verglach ginn.
3, derbäi bekannte Substanzen fir d'Peak Héicht Method ze erhéijen
Wann et vill Komponenten an der onbekannter Probe sinn, sinn déi kritt chromatografesch Peaks ze dicht fir einfach mat der uewe genannter Method z'identifizéieren, oder wann déi onbekannt Probe nëmme fir déi spezifizéiert Artikelanalyse benotzt gëtt.
"Fir d'éischt gëtt e Chromatogramm vun enger onbekannter Probe gemaach, an duerno gëtt e weidere Chromatogramm kritt andeems eng bekannt Substanz un déi onbekannt Probe bäigefüügt gëtt."Komponente mat verstäerkten Héichten kënnen fir sou Substanzen bekannt sinn.
4. Behalen déi qualitativ Method vum Index
De Retentiounsindex representéiert d'Retentiounsverhalen vu Substanzen op Fixativen an ass am Moment dee verbreetsten an international unerkannten qualitative Index am GC.Et huet d'Virdeeler vu gudder Reproduzéierbarkeet, eenheetleche Standard a klenge Temperaturkoeffizient.
De Retentiounsindex ass nëmme mat den Eegeschafte vun der stationärer Phase an der Kolonntemperatur verbonnen, awer net mat aneren experimentellen Bedéngungen.Seng Genauegkeet a Reproduktioun sinn excellent.Soulaang d'Kolonntemperatur d'selwecht ass wéi déi vun der stationärer Phase, kann de Literaturwäert fir d'Identifikatioun applizéiert ginn, an et ass net néideg fir de pure Material fir de Verglach ze benotzen.
(2) Quantitativ Analyse
Basis fir chromatographesch Quantifikatioun:
D'Aufgab vun der quantitativer Analyse ass d'Honnert vun de Komponenten an der gemëschter Probe ze fannen
Fraktioun Inhalt.Chromatographic quantification war baséiert op de folgende: wann Betribssystemer Konditiounen waren konsequent, war
D'Mass (oder d'Konzentratioun) vun der gemoossene Komponent gëtt duerch d'Äntwertsignal vum Detektor bestëmmt
Et ass proportional.Nämlech:
Basis fir chromatographesch Quantifikatioun:
D'Aufgab vun der quantitativer Analyse ass d'Honnert vun de Komponenten an der gemëschter Probe ze fannen
Fraktioun Inhalt.Chromatographic quantification war baséiert op de folgende: wann Betribssystemer Konditiounen waren konsequent, war
D'Mass (oder d'Konzentratioun) vun der gemoossene Komponent gëtt duerch d'Äntwertsignal vum Detektor bestëmmt
Et ass proportional.Nämlech:
1. Peak Area Mooss Method
Peak Beräich ass déi Basis quantitativ Daten, déi vu Chromatogramme geliwwert ginn, an d'Genauegkeet vun der Peakflächmiessung beaflosst direkt d'quantitativ Resultater.Verschidde Miessmethoden goufen fir chromatografesch Peaks mat verschiddene Peakformen benotzt.
Et ass schwéier de genaue Wäert vum Wanter a quantitativer Analyse ze fannen:
Engersäits wéinst der Schwieregkeet den absoluten Injektiounsvolumen genau ze moossen: op der anerer Säit
D'Spëtztfläch ass ofhängeg vun de chromatographesche Bedéngungen, an de chromatografesche Sträif soll erhale bleiwen wann de Wäert gemooss gëtt.
Et ass weder méiglech nach bequem datselwecht ze maachen.An och wann Dir kënnt et richteg kréien
De genaue Wäert, och well et kee vereenegt Standard gëtt a kann net direkt applizéiert ginn.
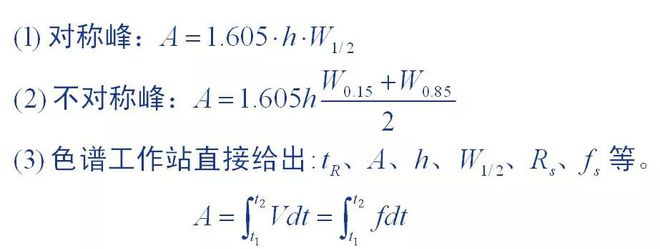
2.Quantitative Korrekturfaktor
Definitioun vu quantitative Korrekturfaktor: Betrag vun Komponenten déi an den Detektor erakommen (m)
De Verhältnis vu sengem chromatografesche Peakgebitt (A) oder Peak Héicht () ass eng Proportionalitéitskonstant (,
D'Proportionalitéitskonstant gëtt den absolute Korrekturfaktor fir de Komponent genannt.
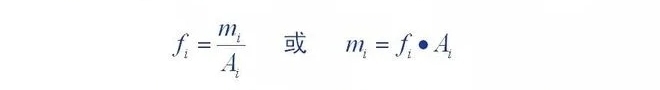
Et ass schwéier de genaue Wäert vum Wanter a quantitativer Analyse ze fannen:
Engersäits wéinst der Schwieregkeet den absoluten Injektiounsvolumen genau ze moossen: op der anerer Säit
D'Spëtztfläch ass ofhängeg vun de chromatographesche Bedéngungen, an de chromatografesche Sträif soll erhale bleiwen wann de Wäert gemooss gëtt.
Et ass weder méiglech nach bequem datselwecht ze maachen.An och wann Dir kënnt et richteg kréien
De genaue Wäert, och well et kee vereenegt Standard gëtt a kann net direkt applizéiert ginn.
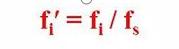
Dat ass, de relativen Korrekturfaktor 'vun engem Komponent ass de Komponent an d'Referenzmaterial s
D'Verhältnis vun den absolute Korrekturfaktoren.
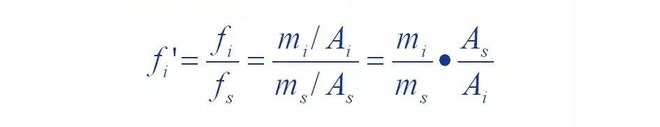
Et kann gesi ginn datt de relativen Korrekturfaktor ass wann d'Qualitéit vun der Komponent versus de Standard ass.
Wann d'Substanz s gläich ass, ass d'Spëtztfläch vum Referenzmaterial d'Spëtztfläch vun der Komponent
Multiple.Wann e puer Komponente Mass m an Héichpunkt Beräich A huet, dann d'Zuel vun f'A
Wäerter sinn gläich op d'Spëtzt Beräich vun der Referenz Material mat Mass vun.An anere Wierder,
Duerch de relativen Korrekturfaktor kënnen d'Spëtzegebidder vun all Komponent getrennt ginn
Ëmgerechent an d'Spëtztfläch vum Referenzmaterial gläich wéi seng Mass, dann de Verhältnis
De Standard ass vereenegt.Also ass dëst déi normaliséiert Method fir de Prozentsaz vun all Komponent erauszefannen
D'Basis vun der Quantitéit.
Methode fir relativ Korrektur Faktor ze kréien: relativ Korrektur Faktor Wäerter waren nëmmen am Verglach mat Wiesen
D'Miessung ass am Zesummenhang mam Standard an der Aart vum Detektor, awer mam Operatiounsstreifen
Et ass egal.Dofir kënne Wäerter aus Referenzen an der Literatur zréckgezunn ginn.Wann den Text
Wann Dir de gewënschte Wäert net an der Offer fannt, kënnt Dir et och selwer bestëmmen.Method vun Bestëmmung
Method: Eng gewësse Quantitéit vum gemoossene Substanz zéng ausgewielte Referenzmaterial → zu enger bestëmmter Konzentratioun gemaach
D'chromatographic Biergspëtzten Beräicher A an As vun den zwee Komponente goufen gemooss.
Dat ass d'Formel.
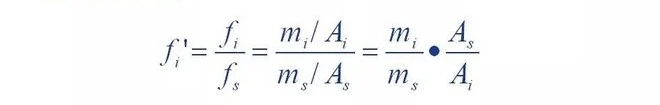
3. Quantitativ Berechnung Method
(1) Area Normaliséierung Method
D'Zomm vum Inhalt vun all de Peak-fräie Fraktiounen gouf als 100% fir d'Quantifizéierung berechent
D'Methode gëtt Normaliséierung genannt.Seng Berechnungsformel ass wéi follegt:
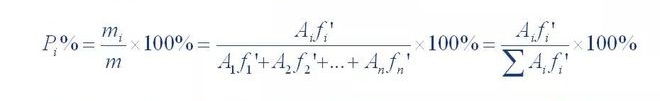
Wou P,% de Prozentsaz Inhalt vun de getest Komponente ass;A1, A2 ... A n ass Komponent 1. D'Spëtztfläch vun 1~n;f'1, f'2 ... f'n ass de relativen Korrekturfaktor fir Komponenten 1 bis n.
(2) extern Standard Method
D'Methode vum quantitative Verglach tëscht dem Äntwertsignal vun der Komponent, déi an der Probe getest gëtt, an der reiner Komponent, déi als Kontroll getest gëtt.
(3) Intern Standard Method
Déi sougenannt intern Standardmethod ass eng Method, an där eng gewësse Quantitéit u reiner Substanz un d'Standardléisung vun der getestter Substanz an der Probeléisung als intern Standard bäigefüügt gëtt, an dann analyséiert a bestëmmt gëtt.
(3) Standard Additioun Method
D'Standardadditiounsmethod, och bekannt als intern Zousatzmethod, ass eng gewësse Quantitéit vun (△C) derbäi ze ginn.
D'Referenz vun der Testsubstanz gouf an d'Proufléisung bäigefüügt fir ze testen, an den Test gouf an den Assay bäigefüügt
Den Héichpunkt vun der Proufléisung no der Substanz war méi héich wéi dee vun der ursprénglecher Proufléisung
D'Erhéijung vum Beräich (△A) gouf benotzt fir d'Konzentratioun vun der Substanz an der Proufléisung ze berechnen
Inhalt (Cx)
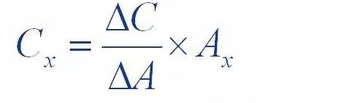
Wou Axe d'Spëtztfläch vun der Substanz ass, déi an der ursprénglecher Probe gemooss gëtt.

Post Zäit: Mar-27-2023